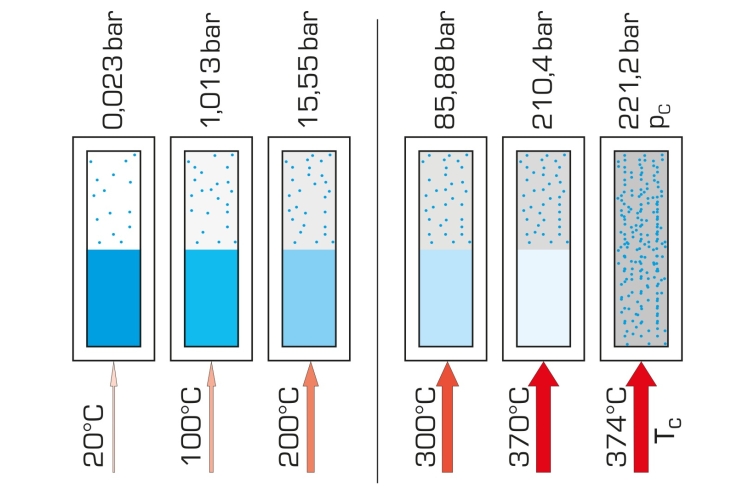
En un sistema cerrado lleno de líquido se ajusta un equilibrio termodinámico entre el líquido y su fase vaporizada. La presión existente se denomina presión de vapor. Esta depende de la materia y la temperatura.
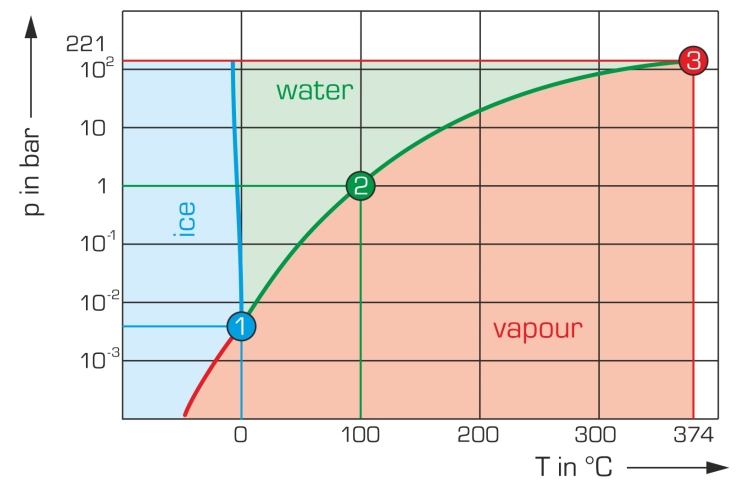
Al calentar un líquido en un depósito cerrado, la presión aumenta con el aumento de la temperatura. En teoría, el aumento de presión es posible hasta el punto crítico, en el cual las densidades de la fase líquida y gaseosa se igualan. El líquido y el vapor ya no se pueden diferenciar.
Este conocimiento encuentra su aplicación práctica en la ingeniería de procesos en la liofilización o la cocina a presión.
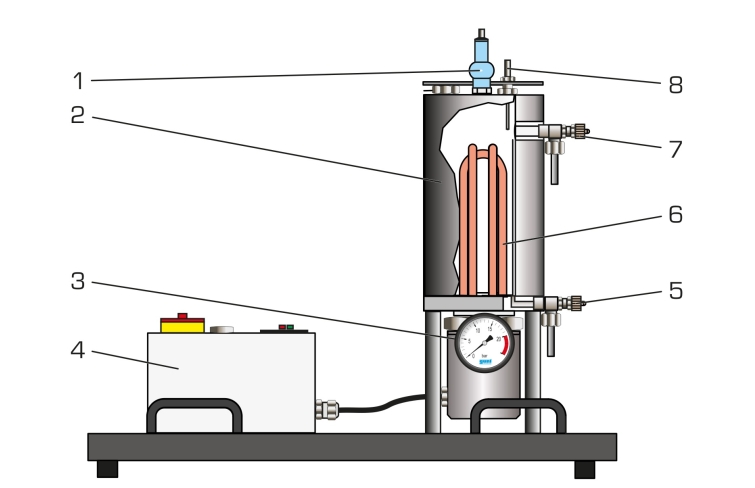
Con el equipo de ensayo WL 204 se puede demostrar fácilmente la relación entre la presión y la temperatura para el caso del agua. Para registrar la curva de presión de vapor son posibles temperaturas de hasta 200°C. La temperatura y la presión se pueden observar continuamente a través de un indicador de temperatura digital y un manómetro de Bourdon, respectivamente.
Como dispositivo de seguridad, el equipo dispone de un regulador de temperatura y una válvula de seguridad, que protege al sistema de la alta presión.